SONNO E METABOLISMO: QUALE RELAZIONE?

ESISTE UNA RELAZIONE TRA METABOLISMO E SONNO?
Durante la prima visita, chiedo spesso ai clienti informazioni sulla qualità e durata del sonno. È frequente scoprire che dormono meno di 8 ore, il sonno non è ristoratore, è intermittente e difficile da riprendere. Pochi sanno che la qualità del sonno, insieme a esercizio fisico e corretta alimentazione, ha un grande impatto sulla salute e sulle condizioni metaboliche. Sonno e metabolismo sono strettamente correlati.
La sindrome da sonno insufficiente e la privazione del sonno sono incluse nella classificazione internazionale dei disturbi del sonno (ICSD-10). Un sondaggio condotto nel 2013 dalla National Sleep Foundation ha rivelato che il 21% degli intervistati negli Stati Uniti dorme meno di 6 ore durante i giorni lavorativi. Numerosi studi epidemiologici hanno evidenziato un legame tra la riduzione delle ore di sonno e un aumento del rischio di diabete di tipo 2, obesità e malattie cardiovascolari.
Se da una parte la restrizione del sonno aumenta il dispendio energetico a causa dell’aumentata insonnia, dall’altra può portare ad una serie di squilibri metabolici che verrebbero ad instaurarsi in seguito ad un aumento sproporzionato dell’assunzione di cibo, ad una diminuzione dell’attività fisica e all’aumento di peso. Pertanto la qualità e la durata del sonno non possono essere considerati degli elementi secondari di poco conto per quello che riguarda il nostro benessere quotidiano, rientrando tra i fattori di rischio per l’aumento di peso, l’obesità e l’instaurarsi di uno stato infiammatorio. Quando questi disordini metabolici sono già presenti, i disturbi del sonno dovrebbero essere corretti in modo opportuno per evitare che diventino ulteriori fattori di rinforzo delle patologie già in atto.
IL SONNO E LE CONSEGUENZE DELLE SUE ALTERAZIONI
Il sonno è uno stato naturale caratterizzato da alterazioni della coscienza, inibizione dell’attività sensoriale e riduzione del movimento muscolare volontario. Si divide in sonno rapido (REM) e sonno non-rapido (NREM), quest’ultimo suddiviso in tre fasi: N1, N2 e N3. Nella fase N1, il tono muscolare è attivo con movimenti lenti degli occhi. In N2, i dormienti sono più difficili da svegliare. Nella fase N3, la sensibilità agli stimoli esterni è ridotta. Il sonno REM è caratterizzato da rapidi movimenti oculari e atonia muscolare. Un sonno sano comprende quattro o cinque cicli di 90 minuti di NREM e REM per notte, con NREM predominante all’inizio e REM verso la fine.
Il sonno è regolato da due processi principali, il processo circadiano e l’azionamento omeostatico del sonno, che aumenta con la veglia e diminuisce durante il sonno. Negli esseri umani, l’impulso per il sonno può essere annullato dalla restrizione volontaria o interrotto da fattori ambientali o disturbi come apnea ostruttiva del sonno (OSA), insonnia, sindrome delle gambe senza riposo e narcolessia.
Studi epidemiologici hanno dimostrato che dormire 6-7 ore a notte è associato a obesità, diabete, malattie cardiovascolari e mortalità. L’analisi dello studio NHANES ha mostrato un legame tra il sonno ≤5 ore e il pre-diabete. Nelle persone con sonno breve, indipendentemente dal BMI, sono state osservate variazioni ormonali come una diminuzione della leptina e un aumento della grelina che suggeriscono che questi cambiamenti promuovono un’alimentazione eccessiva e aumentano il rischio di obesità.
Nelle persone che dormivano meno di 8 ore, l’aumento del BMI era proporzionale alla diminuzione del sonno. Il legame tra sonno breve e obesità è stato supportato da uno studio di 16 anni in cui le donne che dormivano 5 ore o meno hanno guadagnato 1,14 kg in più rispetto a quelle che dormivano 7 ore. Il disturbo del sonno è un problema serio per chi lavora su turni poiché il lavoro notturno è associato a un sonno breve (in media 4,8 ore).
Uno studio su 1.806 lavoratori ha mostrato un rischio relativo di malattia coronarica nei lavoratori a turni di 1,5 rispetto ai lavoratori diurni. In uno studio su 2.860 lavoratori maschi, il rischio relativo di diabete di tipo 2 per i lavoratori a turni è aumentato rispetto ai diurni. Inoltre, su 4.328 lavoratori valutati, il lavoro a turni è un fattore di rischio per l’aumento di peso. Studi osservazionali hanno mostrato un’associazione tra OSA, narcolessia, insonnia e sindrome delle gambe senza riposo con insulino-resistenza e ridotta tolleranza al glucosio.
GLI EFFETTI BIOLOGICI DELLA MODIFICHE DEL SONNO
I processi biologici influenzati dalle variazioni quantitative e qualitative del sonno sono diversi e li possiamo così riassumere:
- Modifiche ormonali: i disturbi del sonno possono alterare la produzione di ormoni come quello della crescita, della prolattina, del testosterone, modificare le preferenze, i tempi e le quantità di assunzione del cibo, abbassare la tolleranza al glucosio e aumentare la resistenza all’insulina. Un debito di sonno può far ridurre l’ormone leptina, che ha un ruolo anoressizzante, e aumentare l’ormone grelina, dal ruolo opposto, oltre che spostare la scelta alimentare a preferire cibi più calorici e ricchi di carboidrati. E’ stato dimostrato che non solo la diminuzione della durata del sonno, ma anche della qualità del sonno influisce negativamente sulla regolazione della glicemia. Gli effetti della frammentazione del sonno sulla regolazione del glucosio sono stati studiati interrompendo il sonno utilizzando stimoli uditivi e meccanici (vibrazioni) indipendentemente dallo stadio del sonno (30/h). Dopo due notti di frammentazione del sonno, la sensibilità all’insulina valutata dall’IVGTT è risultata diminuita e il cortisolo mattutino è aumentato. Uno studio diverso ha valutato l’effetto dell’interruzione specifica dello stadio del sonno sul controllo del glucosio. La soppressione delle onde lente per 3 notti, senza cambiamenti significativi nel tempo di veglia e il tempo di sonno totale, ha portato a una diminuzione della sensibilità all’insulina senza aumento compensativo del suo rilascio. L’OSA è un disturbo del sonno che combina la frammentazione del sonno e l’ipossiemia (riduzione apporto di ossigeno). Oltre agli effetti avversi della frammentazione del sonno e della diminuzione della sua qualità, è stato dimostrato che l’ipossiemia stessa influisca negativamente sul metabolismo del glucosio. L’ipossiemia intermittente, indotta sperimentalmente in 13 volontari sani per 5 ore durante la veglia rispetto alla normossia, ha determinato una diminuzione della sensibilità all’insulina come valutato dall’IVGTT. Sapendo che la frammentazione del sonno compromette anche la sensibilità all’insulina, l’ipossia durante l’OSA può aumentare tale effetto e contribuire allo sviluppo del diabete. Nelle persone diabetiche risulta pertanto importante la gestione delle OSA come trattamento collaterale al dismetabolismo glucidico.
- Modifiche genetiche e della risposta infiammatoria: alterazioni genetiche come la modificazione della cromatina, la regolazione dell’espressione genica, il metabolismo macromolecolare e le risposte infiammatorie, immunitarie e di stress si possono avere in seguito a modifiche del sonno. L’effetto della perdita del sonno sulle citochine infiammatorie è stato valutato in uno studio con privazione del sonno totale di 50 ore, in cui la perdita di sonno ha causato un aumento della citochina pro-infiammatoria TNF-alfa rispetto a una notte di sonno di 8 ore al basale, ma nessuna modifica dell’interleuchina-6, del cortisolo o della PCR . La restrizione parziale del sonno, a 4 ore per 5 notti rispetto a un gruppo di controllo che dormiva 8 ore/notte, ha portato a variazioni dell’espressione di RNA leucocitaria valutata da microarray del genoma completo. La limitazione del sonno ha alterato l’espressione di 117 geni: 15 dei 25 geni più espressi includevano quelli per l’attivazione delle cellule B, per la produzione di interleuchina-8 e per la segnalazione NF-kB. Se tale attivazione viene mantenuta durante una prolungata sospensione parziale del sonno, si potrebbe attivare un’infiammazione cronica di basso livello che potrebbe contribuire a condizioni di salute rischiose incluse la malattie cardiometaboliche.
- Timing del sonno e regolazione del glucosio: oltre agli effetti della quantità e della qualità del sonno, anche i tempi del sonno sembrano avere un effetto sulla regolazione del glucosio. Un disallineamento del ritmo circadiano conseguente a un’inversione del ciclo sonno/veglia e digiuno/alimentazione può comportare un aumento della glicemia postprandiale nonostante un aumento dell’insulina, una diminuzione della leptina, una riduzione dell’efficienza del sonno e un’inversione del profilo di cortisolo e melatonina relativi al ciclo comportamentale. In uno studio una condizione di disallineamento circadiano combinato di 2,5 settimane più una restrizione del sonno (5,6 ore TIB/24 ore) rispetto a un TIB di 10 ore al basale e 9 giorni di recupero con 10 ore di TIB, ha portato ad un aumento del glucosio e ad una diminuzione delle concentrazioni di insulina dopo un pasto misto, indicando una diminuzione della funzione delle cellule beta pancreatiche. Per verificare direttamente se il disallineamento circadiano di per sé abbia effetti negativi sul metabolismo, è stato confrontato l’effetto della combinazione di disallineamento circadiano e perdita del sonno rispetto allo stesso grado di perdita del sonno da solo. La limitazione del sonno a 5 ore TIB/24 ore per 8 giorni ha ridotto la sensibilità all’insulina rispetto al basale in entrambe le condizioni allineate e disallineate.
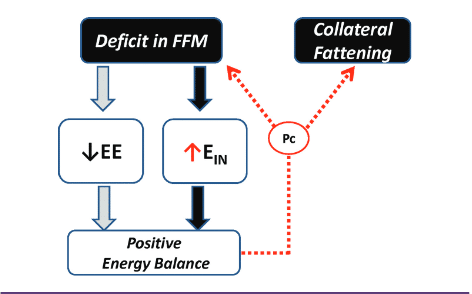
L’immagine sottostante schematizza la relazione tra sonno e metabolismo.

SONNO E METABOLISMO: CONCLUSIONI
La limitazione del sonno da sola o in combinazione con il disallineamento e la diminuzione della qualità dello stesso, influenzano negativamente la regolazione del glucosio. La riduzione del sonno altera il dispendio energetico, la regolazione del peso, l’espressione genica e i livelli di citochine infiammatorie. Gli effetti della limitazione del sonno sono osservati in individui sani di età e sesso diversi e in pazienti con patologie come il diabete di tipo 1. Nei pazienti con apnea ostruttiva del sonno, la combinazione di sonno interrotto con ipossia può avere effetti ancora peggiori sul metabolismo del glucosio.
L’effetto del sonno sulla progressione di molte altre condizioni mediche e il loro trattamento è ancora sconosciuto. Nonostante la prova convincente per gli effetti deleteri di una riduzione della qualità e quantità del sonno, vi è ancora una scarsità di ricerche scientifiche per testare il miglioramento del sonno come un approccio terapeutico nel migliorare la salute metabolica nei soggetti che hanno acquisito o sono a rischio di sviluppare obesità, diabete, o malattia cardiovascolare. Alla luce di tali dati scientifici invece si comprende come la gestione dei disturbi del sonno attraverso tecniche di rilassamento, modifiche dello stile di vita, farmaci o fitoterapici, dovrebbe essere prioritaria sia come prevenzione che come trattamento integrato delle patologie metaboliche e infiammatorie.
Ottieni i Risultati che vuoi!
Iniziamo questo viaggio insieme, verso la tua consapevolezza alimentare.
valentina.rossi91.dietista@gmail.com
+39 3913995856
Fonte: Metabolic effects of sleep disruption, links to obesity and diabetes https://insights.ovid.com/article/01266029-201408000-00008